Transcriptòmica: Sota el nom de covid persistent hom inclou tot un ventall de seqüeles post-agudes de la infecció per SARS-CoV-2. La covid persistent és un condició debilitant, clínicament heterogènia i d’etiologia poc conegudes. Un grup d’investigadors de la Icahn School of Medicine at Mount Sinai, encapçalat per Ryan C. Thompson, i coordinat per Alexander W. Charney i Noam D. Beckmann han realitzat una investigació transcriptòmica de 165 pacients hospitalitzats per covid-19 a qui feren després un seguiment clínic en el període post-agut. Ara la revista Nature Medicine en publica un article en el que Thompson et al. conclouen que les signatures d’expressió gènica de les seqüeles post-agudes ja eren presents en el transcriptoma sanguini durant la infecció aguda. Aquest transcriptoma sanguini és un reflex de cèl·lules del sistema immunitari innat i adaptatiu. Les seqüeles es poden agrupar en dos clústers. En la primera agrupació figuren seqüeles associades a una major expressió de gens relacionats amb la immunoglobulina, d’una manera dependent als títols d’anticossos específics contra la proteïna S del SARS-CoV-2. En la segona agrupació, les seqüeles s’associen a una expressió inferior de gens relacions amb la immunoglobulina, sense dependència dels anticossos anti-S. En una cohort externa aquesta relació ha estat validada. Així doncs, la múltiple etiologia de les seqüeles post-agudes de la covid ja seria detectable durant la infecció aguda.
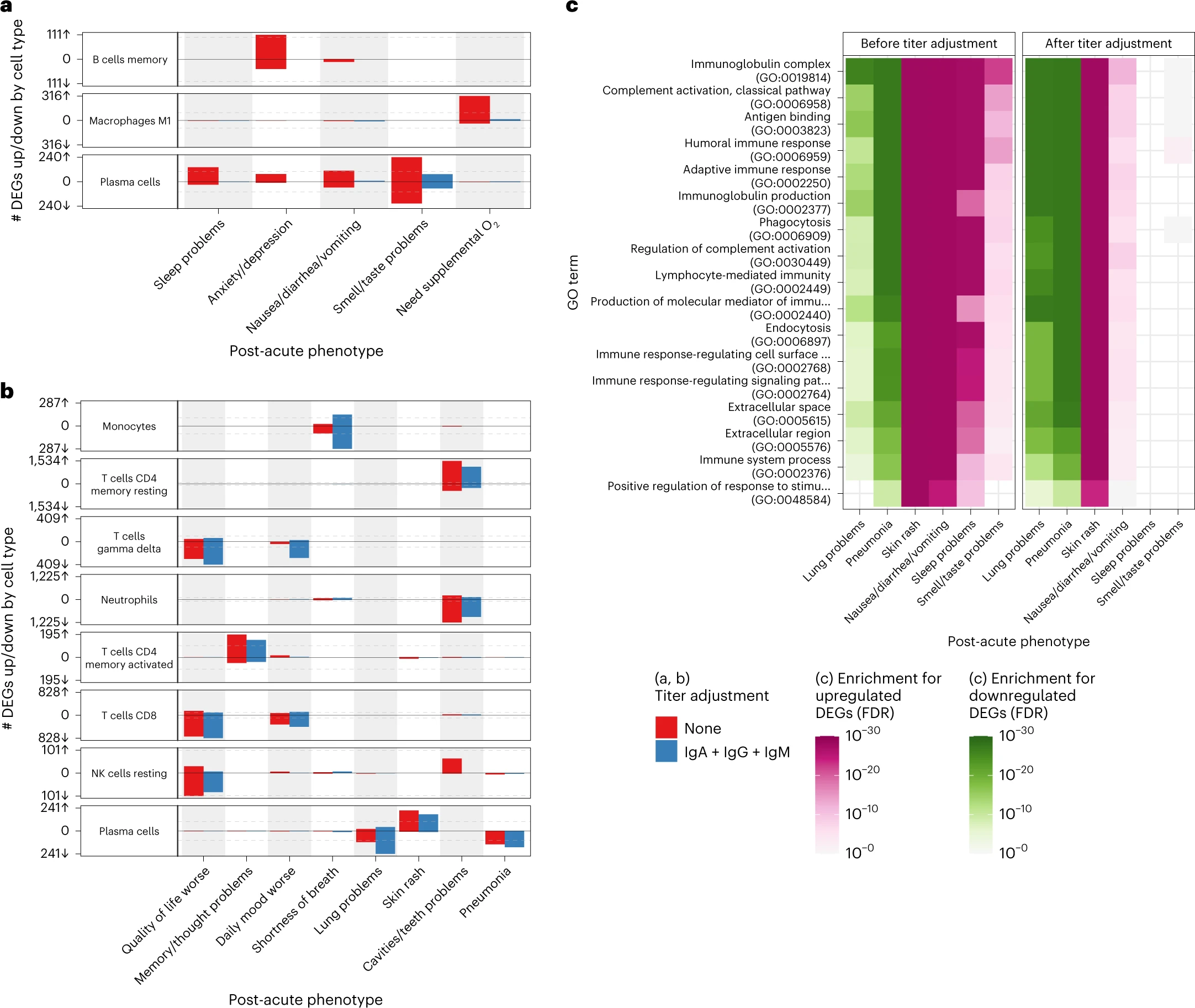
Relació entre els símptomes post-aguts de covid-19 i la transcripció de diversos grups de gens
Les seqüeles de la covid-19
A hores d’ara s’han registrat al món més de 600 milions de casos de covid-19. Una fracció d’aquests casos arrossega seqüeles post-agudes en forma de fatiga, dispnea, anòsmia, etc. Hom pensa que aquests símptomes post-aguts són el resultat d’elements de la resposta del sistema immunitari a la infecció per SARS-CoV-2.
En aquest estudi, Thompson et al. obtingueren perfils d’expressió gènica i de títol d’anticossos en sang de pacients hospitalitzats per covid-19 a qui seguiren clínicament en el període post-agut. En els pacients s’identificaren signatures d’expressió gènica específiques de tipus cel·lular en la fase aguda de la infecció que vinculaven diversos tipus de cèl·lules immunitària a seqüeles post-agudes presents un any després de l’alta hospitalària. Com a mínim, hi hauria dues etiologies independents entre elles, una de les quals seria dependent dels nivells d’anticossos anti-S desenvolupats en la fase aguda de la infecció.
Un estudi transcriptòmic amb 567 individus en el marc del biobanc de Mount Sinai
Entre abril i juny del 2020 foren recrutats al Mount Sinai COVID-19 Biobank Study 567 individus, incloent-hi 495 persones hospitalitzades per covid-19 i 72 controls (alguns d’ells sans i d’altres de pacients hospitalitzats per altres causes). La sang era recollida en el cas dels pacients hospitalitzats durant l’estada, i en el cas dels controls sans en una visita externa. En total es realitzaren 1.392 seqüenciacions d’ARN.
Una fracció dels pacients que van rebre l’alta hospitalària foren visitats més de sis mesos després de l’alta, i se’ls oferí de respondre una enquesta sobre símptomes post-aguts. L’enquesta fou resposta per 232 individus (amb una mediana de 363 dies després de l’alta hospitalària), dels quals de 165 n’hi havia dades de RNA-seq de la fase aguda.
Entre aquests 165 individus, n’hi havia 50 dels qual es disposava la data d’administració de la primera dosi de vaccí anti-covid-19. Entre aquests 50 no s’hi trobà cap associació significativa entre haver rebut el vaccí i la simptomatologia post-aguda. Dels 165 individus, n’hi hagué 14 que reportaren reinfeccions.
Entre els pacients hospitalitzats inclosos en aquest estudi no s’observa una associació entre la severitat de la fase aguda o l’ingrés a una unitat de cures intensives i els símptomes post-aguts. Tampoc no hi ha una associació pel que fa a l’edat. Sí que hi ha una relació entre el sexe i la pèrdua de cabell com a símptoma post-agut. També hi ha algunes associacions amb comorbiditats prèvies, medicacions rebudes en la fase aguda i alguns resultats de laboratori (del total de 2780 tests realitzats). Hi ha una associació interessant entre problemes de son i els nivells d’anticossos anti-S en la fase aguda.
Dels 165 individus, Thompson et al. disposaven de dades de RNA-seq de 361 mostres de sang preses en la fase aguda. Amb eines bioinformàtiques es possible relacionar les dades transcriptòmiques amb les diferents fraccions de tipus cel·lular presents a la sang. Així doncs, per exemple, uns nivells superiors de cèl·lules plasmàtiques i uns nivells inferiors de cèl·lules T auxiliars fol·liculars en la fase aguda s’associen amb símptomes post-aguts de pneumònia i de miàlgia, respectivament.
Les cèl·lules plasmàtiques presenten un mínim de 100 gens amb expressió diferencials segons el major nombre de símptomes (problemes de son, problemes pulmonars, problemes digestius, problemes cutanis, problemes d’olfacte i de gust, etc.). També tenen força rellevància les cèl·lules T CD8+ i γδ, amb gens d’expressió diferencial vinculats a una pitjor qualitat de vida. Les cèl·lules T CD4+ de memòria en repòs i els neutròfils s’associaven amb problemes dentaris. Les cèl·lules T CD4+ de memòria activades s’associaven amb problemes cognitius.
D’acord amb els patrons d’expressió gènica de la fase aguda es possible dividir els símptomes post-aguts en dos grups:
- grup pulmonar de cèl·lula plasmàtica: problemes pulmonars i pneumònia.
- grup miscel·lani de cèl·lula plasmàtica: problemes de son, digestius, cutanis i d’olfacte i gust.
La principal diferència entre aquests dos grups és que els gens relacionats amb la immunoglobulina es troben reprimits en el primer grup i sobreexpressats en el segon grup.
La funció principal de cèl·lules plasmàtiques és la producció d’anticossos. Per això, Thomson et al. investigaren la relació entre els títols d’anticossos anti-S en la fase aguda i els símptomes post-aguts. Normalitzaren les RNAseq d’acord amb els nivells sanguinis d’IgG, IgA i IgM anti-S. D’aquesta manera discriminaren entre els gens d’expressió diferencial dependents del títol d’anticossos anti-S i els gens d’expressió diferencial independents. El clúster miscel·lani de cèl·lules plasmàtiques quedava atenuat amb aquesta correcció, mostrant doncs la seva dependència del títols d’anticossos anti-S. Els símptomes pulmonars i cutanis, en canvi, resultaven independent d’aquests títols. En canvi aquests símptomes pulmonars i cutanis sí eren dependents dels títols d’anticossos totals, en el sentit que uns menors nivells d’anticossos totals durant la fase aguda de la covid-19 s’associaven a una major simptomatologia pulmonar i cutània en la fase post-aguda.
L’etiologia dels símptomes post-aguts de la covid-19
Com també havien assenyalat altres estudis, Thompson et al. constaten la rellevància de la fase aguda de covid-19 en patogènesi post-aguda de la covid persistent. El tipus cel·lular sanguini més rellevant en aquest estudi són les cèl·lules plasmàtiques. En alguns casos durant la fase aguda de la covid-19 les cèl·lules plasmàtiques reprimeixen l’expressió de gens implicats en la producció i funcionalitat d’anticossos, i això es tradueix en la fase post-aguda en un major risc de patir simptomatologia pulmonar. En altres casos, les cèl·lules plasmàtiques, durant aquesta fase aguda, experimenten una sobreexpressió d’aquests gens, la qual cosa afavoreix l’aparició de símptomes post-aguts diferents com l’anòsmia. En aquesta segona simptomatologia tenen un paper important els nivells aguts d’anticossos específics adreçats contra la proteïna S del SARS-CoV-2.
Lligams:
- Molecular states during acute COVID-19 reveal distinct etiologies of long-term sequelae. Ryan C. Thompson, Nicole W. Simons, Lillian Wilkins, Esther Cheng, Diane Marie Del Valle, Gabriel E. Hoffman, Carlo Cervia, Brian Fennessy, Konstantinos Mouskas, Nancy J. Francoeur, Jessica S. Johnson, Lauren Lepow, Jessica Le Berichel, Christie Chang, Aviva G. Beckmann, Ying-chih Wang, Kai Nie, Nicholas Zaki, Kevin Tuballes, Vanessa Barcessat, Mario A. Cedillo, Dan Yuan, Laura Huckins, Panos Roussos, Thomas U. Marron, The Mount Sinai COVID-19 Biobank Team, Benjamin S. Glicksberg, Girish Nadkarni, James R. Heath, Edgar Gonzalez-Kozlova, Onur Boyman, Seunghee Kim-Schulze, Robert Sebra, Miriam Merad, Sacha Gnjatic, Eric E. Schadt, Alexander W. Charney & Noam D. Beckmann. Nature Medicine (2022)
- Microcoàguls amiloides de fibrina i alteracions plaquetàries en la covid persistent (agost del 2022).
- Fatiga, feblesa muscular, dificultats de la son, ansietat i depressió a 6 mesos de l’alta hospitalària per covid-19 (gener del 2021).
Cap comentari:
Publica un comentari a l'entrada